

Doelen
- Je weet wat een ion is.
- Je weet wat enkelvoudige en samengestelde ionen zijn.
- Je weet hoe het komt dat een ion lading heeft.
- Je kunt bepalen wat de lading van een ion is.
- Je kunt de samenstelling van een ion bepalen.
Ionen
Ionen zijn atomen met een lading. Deze lading wordt veroorzaakt door een verschil in het aantal protonen en het aantal elektronen. In de paragraaf over atomen heb je geleerd dat het aantal elektronen en protonen altijd gelijk moet zijn. Dit geldt niet voor ionen.
Atomen en ionen
Je hebt in de vorige paragraaf geleerd over atomen. Ionen lijken in veel opzichten op atomen. De bouw met een kern en elektronenwolk is hetzelfde. Ook hebben ionen net als atomen een symbool als afkorting voor lange namen.
Het verschil tussen atomen en ionen is de aanwezigheid van een lading die veroorzaakt wordt door een verschil in het aantal positieve protonen en het aantal negatieve elektronen. Het aantal neutronen is gelijk.
Positief en negatief
Ionen hebben een lading en die kan positief of negatief zijn. Dit geef je aan door een + of - schuin boven het symbool te zetten. Het waterstof ion schrijf je als H+. Een negatief Chloor ion schrijf je als Cl-. Als een ion een + of - lading heeft schrijf je alleen een + of - boven het symbool. Er zijn ook ionen die een lading van 2+, 3+, 4+, 2- of 3- hebben. Het zuurstof-ion heeft bijvoorbeeld een lading van 2- en wordt dan O2-. IJzer heeft een lading van 3+ en wordt Fe3+.
Van atoom naar ion.
Om aan een positieve of negatieve lading te komen wordt het aantal elektronen in het atoom veranderd. Het aantal protonen staat vast. Dit bepaald welke stof het is en is gekoppeld aan het atoomnummer en aan het symbool. Het aantal neutronen bepaald samen met de protonen de massa. Het aantal elektronen bepaald de lading.
Als er meer elektronen zijn dan protonen is er een negatieve lading. Chloor heeft 17 protonen en 19 neutronen. Een chloor atoom heeft dus 17 elektronen zodat de 17 P+ en 17 e- elkaar opheffen.
Een chloor ion heeft een lading van 1-. Er is dus 1 elektron extra bij het atoom gekomen. Er zijn nu 17 protonen en 18 elektronen. 17 P+ en 18 e- = lading van 1-.
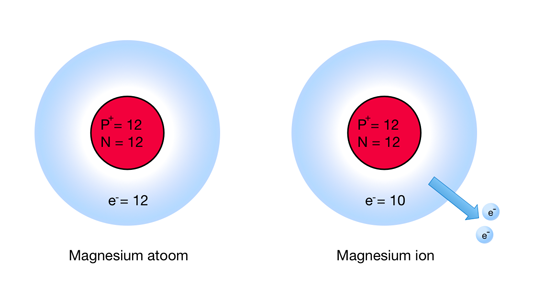
Bij positieve ionen zijn er elektronen tekort waardoor er meer positieve protonen zijn dan negatieve elektronen. Een natrium atoom heeft 11 protonen en 12 neutronen. Er zijn ook 11 elektronen. Maar bij een natrium-ion zijn er maar 10 elektronen. Er is dus 1 elektron minder dan het aantal protonen waardoor de protonen in de meerderheid zijn en er een lading is van 1+.
Lading bepalen
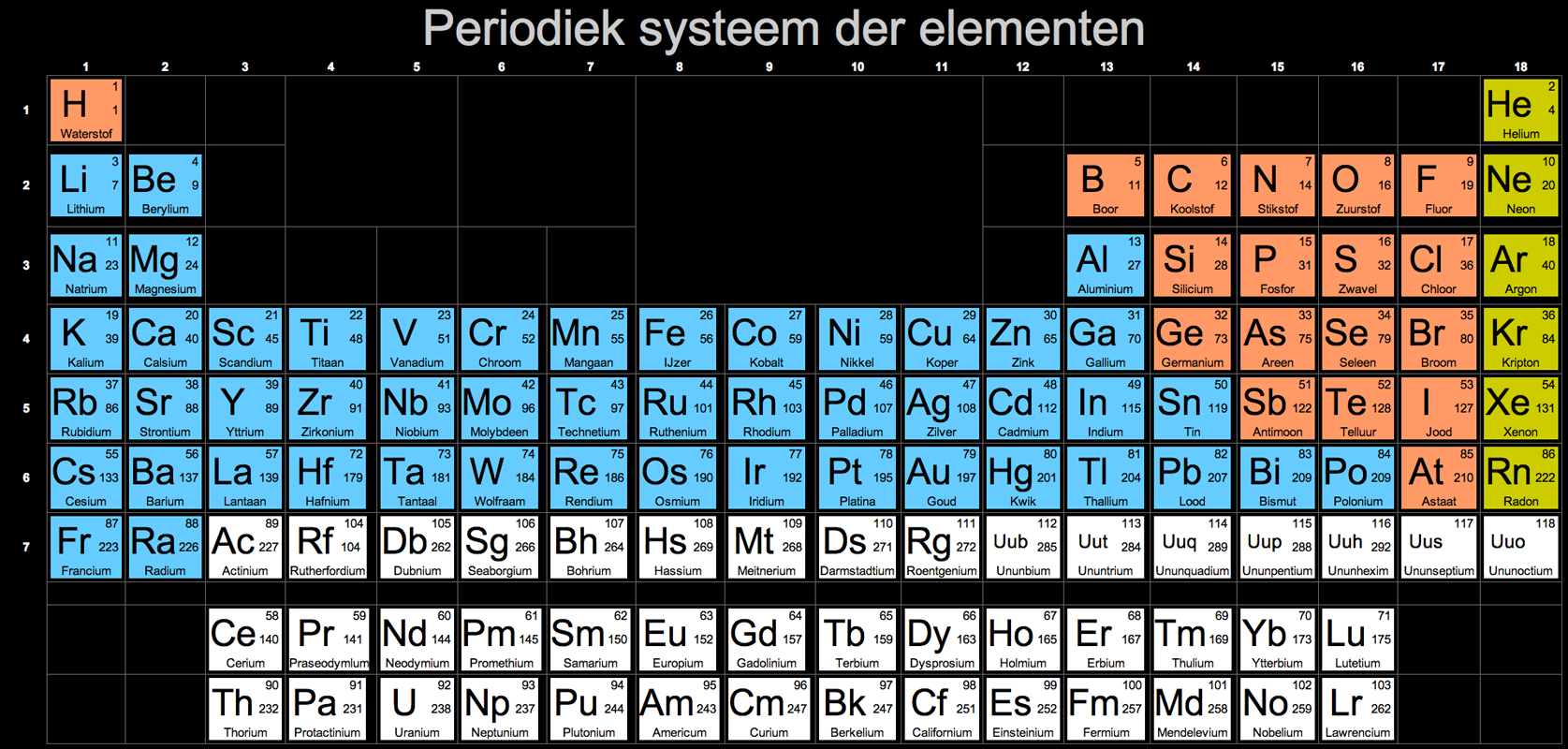
Je kunt met behulp van het periodieksysteem de lading van sommige ionen bepalen. Ook kun je achterhalen of van een atoom ook een ion gevormd kan worden. Het periodieksysteem bestaat uit groepen. Dit zijn de kolommen. Elementen die in dezelfde kolom staan hebben vergelijkbare eigenschappen.
- De eerste groep zijn de alkalimetalen. De ionen van deze elementen hebben een lading van 1+.
- De tweede groep zijn de aardalkalimetalen. Deze krijgen een lading van 2+.
- In de groepen 3 t/m 15 zitten de overgangsmetalen. Deze hebben verschillende positieve ladingen.
- Groep 16 zijn de niet-metalen met een lading van 2-.
- Groep 17 zijn de halogenen met een lading van 1-.
- Van de elementen in groep 18 kun je geen ionen maken. Deze elementen kunnen niet met andere elementen reageren. Dit zijn de edelgassen.
Aantal deeltjes bepalen
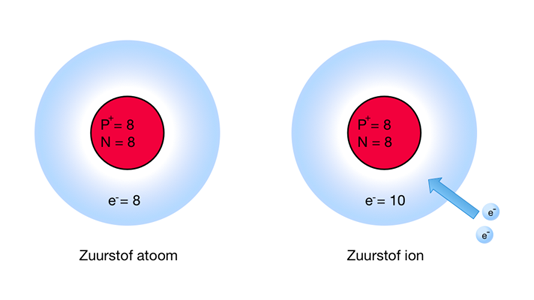
Net als bij atomen kun je met het periodieksysteem bepalen hoeveel protonen, neutronen en elektronen in een ion zitten. Je bepaald eerst het aantal deeltjes die in het atoom zitten. Voor iedere negatieve lading voeg je een elektron toe en voor iedere positieve lading haal je een elektron weg. Een zuurstof atoom heeft:
- 8 protonen
- 8 neutronen
- 8 elektronen
Een zuurstof ion O2- heeft 2 extra elektronen. Het aantal deeltjes wordt dan:
- P+ = 8
- N = 8
- e- = 10
Enkelvoudige en samengestelde ionen
Ionen die uit een atoom voortkomen noemen we enkelvoudige ionen. Er zijn ook ionen die uit een molecuul komen. Deze noemen we samengestelde ionen. Een voorbeeld van een samengesteld ion is het carbonaat ion. CO32-. Dit ion is een molecuul met een lading. In het ion zit 1 koolstof atoom en 3 zuurstof atomen. Er zijn een aantal samengestelde ionen:
- Hydroxide:
OH-
- Nitraat:
NO3-
- Carbonaat:
CO32-
- Sulfaat:
SO42-
- Fosfaat:
PO43-
- Ammonium:
NH4+
Ook voor deze ionen gelden dezelfde regels als bij atomen maar door een tekort of overschot aan elektronen is er een lading.
Wat is een ion?
Wat is het verschil tussen een ion en een atoom?
Welke deeltjes hebben lading?
Welk deeltje heeft geen lading?
Heeft een positief ion meer of minder protonen dan elektronen?
Een ion met een lading 2+ heeft 12 protonen, hoeveel elektronen heeft dit ion?
Een negatief ion met de lading 1- heeft 16 elektronen. Hoeveel protonen heeft dit ion?
Kies de juiste notatie van een beryllium-ion?
a) Be2+
b) Be2+
c) Be2+
d) Be+2
e) 2+Be
f) +2Be
Koper heeft een lading van 2+. Geef de juiste notatie van een koper-ion. Gebruik sketchbook.
Van IJzer bestaat een ion met 2+ en een ion met 3+. We noemen deze stoffen dan IJzer(II) en IJzer(III). Geef de juiste notatie van beide IJzer-ionen.
Wat is de lading van een Mg2+ ion?
Als een Li+ ion 3 protonen heeft, hoeveel elektronen heeft Li+ dan?
Een ion heeft 30 protonen en 28 elektronen. Geef de juiste notatie van dit ion.
Hoeveel protonen heeft een Br- ion?
Hoeveel neutronen heeft een Br- ion?
Hoeveel elektronen heeft een Br- ion?
Een kwik ion heeft 78 elektronen. Wat is de lading van een kwik ion?
Aluminium heeft een lading van 3+. Geef de juiste notatie van een aluminium ion.
Wat is de massa van een aluminium ion?
Geeft de samenstelling van een aluminium atoom. Geef het aantal Protonen, neutronen en elektronen.
Geeft de samenstelling van een aluminium ion. Geef het aantal Protonen, neutronen en elektronen.
Wat kun je zeggen over de eigenschappen van atomen in dezelfde groep?
Wat is de lading van ionen uit groep 1?
Wat is de lading van ionen uit groep 2?
Wat is de lading van ionen uit groep 16?
Wat is de lading van ionen uit groep 17?
Wat kun je zeggen over de lading van ionen uit groep 3 t/m 15?
Wat kun je zeggen over de edelgassen?
Hoe heten de atomen uit groep 17?
In welke groep vindt je de aardalkalimetalen?
Wat is de lading van ionen van de alkalimetalen groep?
Wat is de lading van een zwavel ion?
Geef de samenstelling van een zwavel ion.
Hoeveel neutronen heeft een fosfor ion?
Hoeveel elektronen heeft een seleen ion?
Wat is de lading van een calcium atoom?
Hoeveel elektronen heeft een calcium atoom?
Wat is de lading van een kalium ion?
Hoeveel elektronen heeft een kalium ion?
Geef de samenstelling van een francium atoom.
Geef de samenstelling van een francium ion.
Welke 4 ionen hebben 36 elektronen. (2 positieve en 2 negatieve)
Bestaat een helium ion?
Bestaat een titanium ion?
Wat is een samengesteld ion?
Geef een voorbeeld van een samengesteld ion.
Wat is de lading van een sulfaat ion?
Welke elementen zitten in een carbonaat ion?


